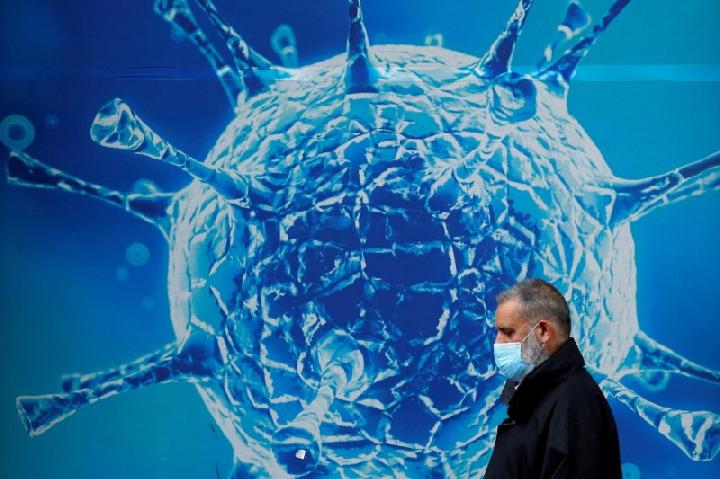
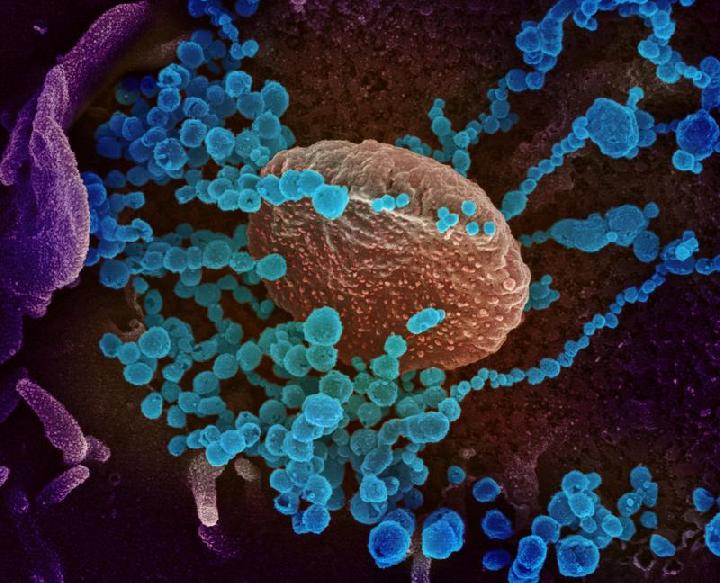
WHO Memvalidasi Vaksin Convidecia untuk Covid-19
Reporter
Maria Fransisca Lahur
Editor
Erwin Prima
Jumat, 20 Mei 2022 14:09 WIB
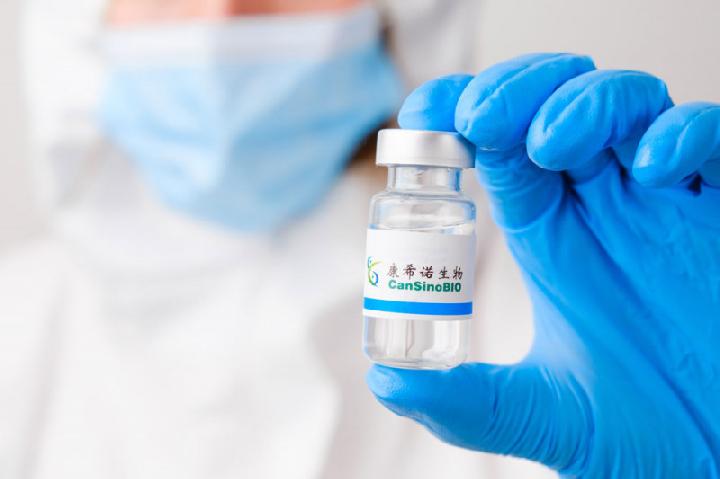
TEMPO.CO, Jakarta - Organisasi Kesehatan Dunia (WHO) mengeluarkan daftar penggunaan darurat (EUL) untuk Convidecia, vaksin yang diproduksi oleh CanSino Biologics, Cina, pada hari Kamis, 19 Mei 2022.
Produk ini menambah portofolio vaksin yang terus bertambah yang divalidasi oleh WHO untuk pencegahan Covid-19 yang disebabkan oleh SARS-CoV-2.
Prosedur EUL WHO menilai kualitas, keamanan, dan kemanjuran vaksin Covid-19 sebagai prasyarat untuk pasokan vaksin COVAX. Prosedur ini juga memungkinkan negara-negara untuk mempercepat persetujuan peraturan mereka sendiri untuk mengimpor dan mengelola vaksin Covid-19.
Convidecia dinilai berdasarkan prosedur EUL WHO berdasarkan tinjauan data tentang kualitas, keamanan, kemanjuran, rencana manajemen risiko, kesesuaian program, dan inspeksi lokasi manufaktur yang dilakukan oleh WHO.
Grup Penasihat Teknis untuk Daftar Penggunaan Darurat, diselenggarakan oleh WHO dan terdiri dari pakar regulasi dari seluruh dunia, telah menentukan bahwa vaksin memenuhi standar WHO untuk perlindungan terhadap Covid-19 dan bahwa manfaat vaksin jauh lebih besar daripada risikonya.
Convidecia didasarkan pada adenovirus manusia yang dimodifikasi yang mengekspresikan protein lonjakan S dari SARS-CoV-2. Ini diberikan sebagai dosis tunggal.
Convidecia juga ditinjau awal bulan ini oleh Kelompok Penasihat Strategis WHO tentang Imunisasi (SAGE), yang merumuskan kebijakan khusus vaksin dan rekomendasi untuk penggunaan vaksin dalam populasi. SAGE merekomendasikan penggunaan vaksin sebagai dosis tunggal (0,5 ml), pada semua kelompok usia 18 tahun ke atas.
Convidecia ditemukan memiliki 64 persen kemanjuran terhadap penyakit simtomatik dan 92 persen terhadap Covid-19 yang parah.
Prosedur daftar penggunaan darurat (EUL) menilai kesesuaian produk kesehatan baru selama keadaan darurat kesehatan masyarakat. Tujuannya adalah untuk membuat obat-obatan, vaksin, dan diagnostik tersedia secepat mungkin untuk mengatasi keadaan darurat sambil mematuhi kriteria keamanan, kemanjuran, dan kualitas yang ketat.
Penilaian mempertimbangkan ancaman yang ditimbulkan oleh keadaan darurat serta manfaat yang akan diperoleh dari penggunaan produk terhadap potensi risiko apa pun.
Jalur EUL melibatkan penilaian yang ketat terhadap data uji klinis fase II dan fase III akhir serta data tambahan substansial tentang keamanan, kemanjuran, kualitas, dan rencana manajemen risiko.
Data ini ditinjau oleh para ahli independen dan tim WHO yang mempertimbangkan badan saat ini bukti tentang vaksin yang sedang dipertimbangkan, rencana untuk memantau penggunaannya, dan rencana untuk studi lebih lanjut.
Sebagai bagian dari proses EUL, perusahaan yang memproduksi vaksin harus berkomitmen untuk terus menghasilkan data untuk memungkinkan lisensi penuh dan prakualifikasi vaksin WHO.
Proses prakualifikasi WHO akan menilai data klinis tambahan yang dihasilkan dari uji coba dan penyebaran vaksin secara bergilir ke memastikan vaksin secara konsisten memenuhi standar kualitas, keamanan, dan kemanjuran yang diperlukan untuk ketersediaan yang lebih luas.
Baca:
Vaksin Covid-19 Dosis Tunggal Buatan Kanada Siap Diuji pada Manusia
Selalu update info terkini. Simak breaking news dan berita pilihan dari Tempo.co di kanal Telegram “Tempo.co Update”. Klik https://t.me/tempodotcoupdate untuk bergabung. Anda perlu meng-install aplikasi Telegram terlebih dahulu.